SCADASCADA(監視制御システム)
SCADAとは
-
SCADA(監視制御システム)は、広範囲に渡る設備やシステムを中央から監視・制御するためのシステムです。さまざまな機器やセンサーから送られるデータを元に、それらを監視・制御しながらデータの蓄積・分析を行います。 上位システム(MESやERP)と生産現場をつなぐ装置としてデータベースを持ち、生産装置やデータ管理・解析、診断情報、電力データ、稼働状況の把握など多くのメリットがあります。 これまで工場や発電所などの大規模な施設で利用され、リアルタイムのデータ収集とプロセス制御で活用されてきました。特にプラントにおいては、故障や異常が発生した場合、迅速な対応が可能になり重宝されてきた監視制御システムです。

SCADAを使用するメリット
SCADA(監視制御システム)の使用は、大規模な施設やシステムの監視と制御に多くのメリットをもたらします。SCADAを使用する場合の主な利点は以下の通りです
-
メリット1
リアルタイムのデータ収集とプロセス制御が可能になり、生産工程全体の精度と一貫性を保証します。
-
メリット2
故障や異常が発生した場合に迅速に対応でき、効率的な運用をサポートします。
-
メリット3
データ収集と記録は規制遵守のために不可欠であり、SCADAはこれを容易にします。
一方、SCADAを使用しない場合、これらの機能と利点を享受することは難しくなります。リアルタイムでの監視と制御が困難になり、異常が発生した場合の対応も遅くなる可能性があります。また、データ収集と記録の手間が増え、それにより規制遵守が困難になる可能性があります。さらに、生産の効率性とコスト削減も影響を受ける可能性があります。
-
SCADAを使用しない場合
データは各装置内に単独で格納されるため、リアルタイムでの分析や監視は困難。それぞれの装置操作はHMIにて単独で操作し稼働する。
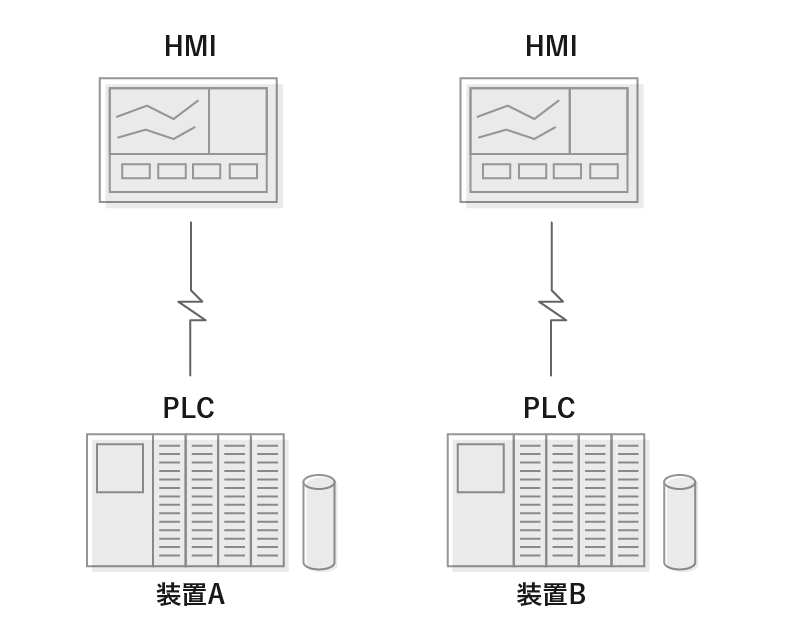
-
SCADAを使用する場合
収集された各装置のデータをSCADA内に統合して格納、リアルタイムでプロセス制御が可能。
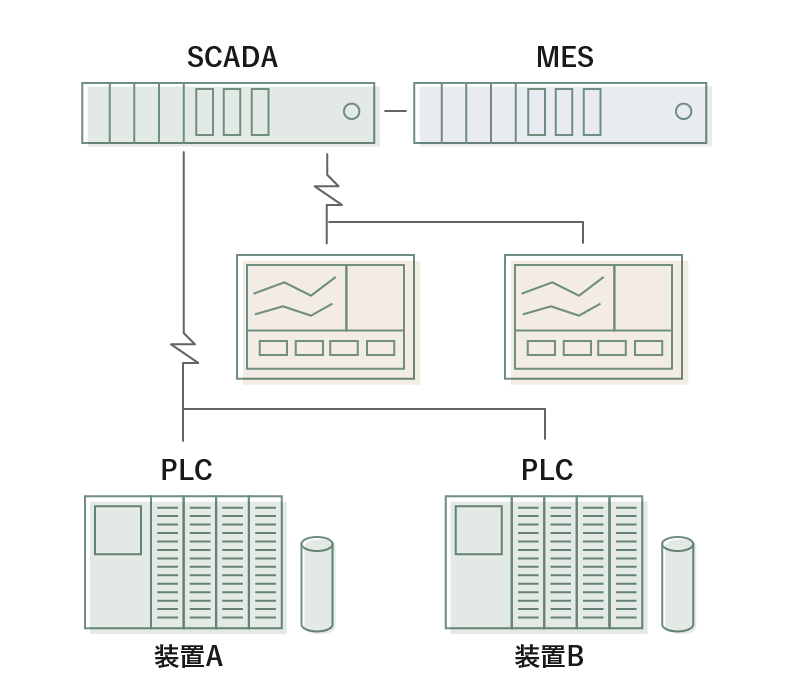
SCADAを製薬業界で活用するメリット
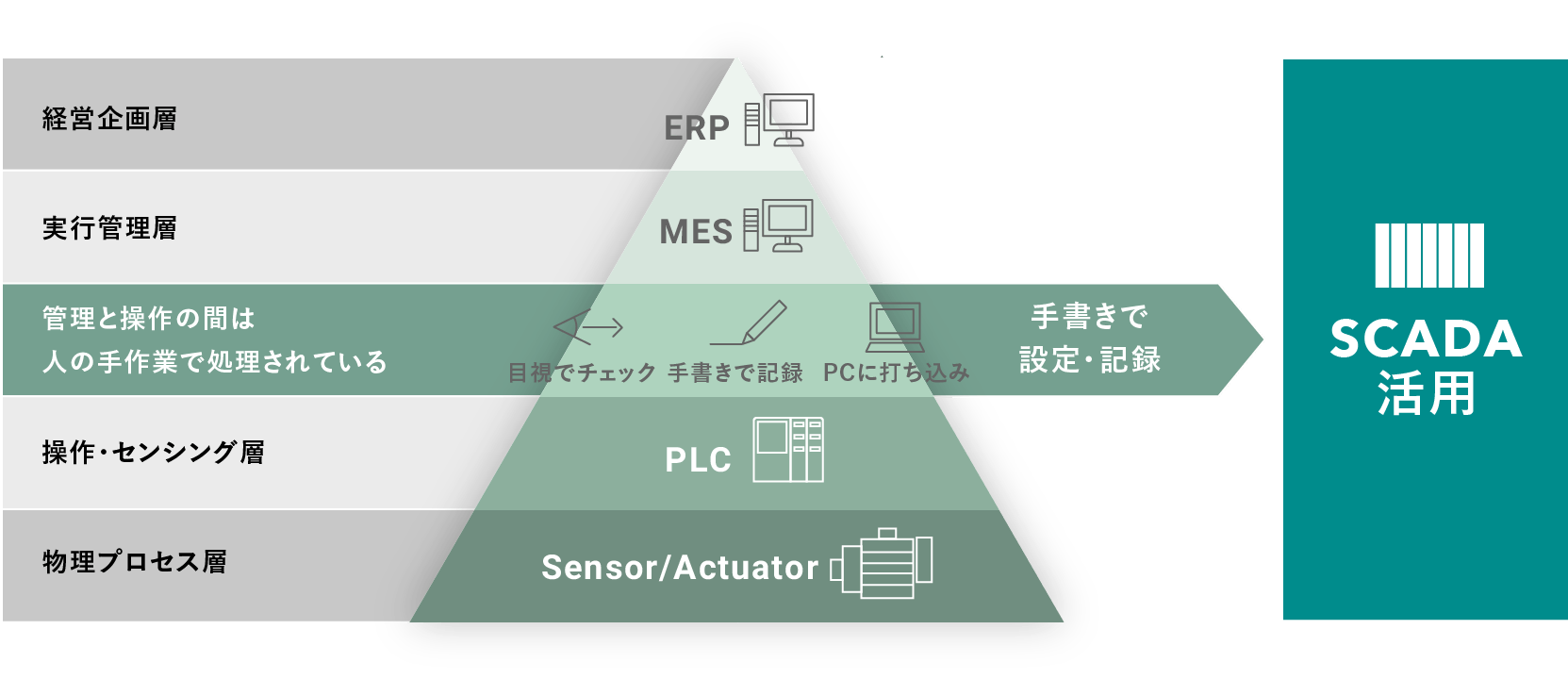
製薬業界においてもSCADAは非常に重要な役割を果たします。医薬品製造プロセスは厳格な品質管理と規制に従わなければなりません。SCADAを活用することでリアルタイムでの監視と制御を可能とし、生産工程全体の精度と一貫性を保証できます。また、データ収集と記録は、GMP等の規制厳守のためには必要不可欠であり、SCADAはこれを容易にします。データの完全性に対する担保と安全性保証のために、デジタル化を推進しデータの信頼性を確保する必要性が高まっています。MESとの連携によりさらなる生産性の向上に寄与します。
国内でのGMP省令の改正や海外査察機関などの締め付け強化もあり、その対策にSCADAを活用しているケースが増えてきています。しかしながら、医薬品製造工場の現状として、まだまだ自動化や電子化が進んでおらず、手書きの書類を採用しているのが現状です。信憑性に疑いはないとして扱われてはいるものの、現実には改ざんされる恐れもあったため、データインテグリティ(データの完全性に対する担保)やパラメトリックリリース(医療品の安全性保証)を重視した電子記録化が求められており、作業履歴やデータ類を全て蓄積できるSCADAが現場の情報基盤として活用され始めています。
IDECファクトリーソリューションズが提供する製品・サービス
製薬業界に最適な「SCADA製品パッケージ」と「システム構築」をトータルで提供します。
SCADA製品パッケージ
- IDECファクトリーソリューションズは、SIEMENS 「SIMATIC SCADA SYSTEM(SIMATIC WinCC Audit)」を提供します。スケーラブルなオープンシステム環境に基づき、生産およびMES/ERPレベルからクラウドソリューションまでのデータを垂直統合するSIMATIC SCADAは、現在の課題だけでなく将来的な課題にも対応できるソリューションの提供が可能です。
各種サブシステムから取得したデータを集約し、独自データベースを構築。一元管理することで、いつでも必要な情報にアクセスできます。また、データマイニングからデータの効率的な分析、目的にあった方法での評価が可能。オペレーションの効率化を目指せます。
IDECファクトリーソリューションズは、シーメンス株式会社のシステムインテグレーションパートナーとして、日本国内で20年以上の実績を積み重ねてきています。 
SIMATIC WinCC Audit(オプションソフトウェア)
- SIEMENS では Part11 遵守に必要な監査証跡を記録するためのオプションソフトウェア SIMATIC WinCC Audit をご用意しています。 特に製薬業界ではGMP(適正製造規範)、21 CFR Part11を遵守するためのガイドラインで定められる監査証跡のユーザー要件に対応が必要です。製薬業界におけるPart11対応における必要な機能であるだけでなく、お客様にとって記録原本の完全性を保証するSIEMENS独自のシステムをご用意しています。
Part11・・・1997 年に FDA(Food and Drug Administration:アメリカ食品医薬品局)が、記録や署名をペーパーレス(電子)による記録の保護、保存を認める為発行された規則。 規則の内容は、「監査証跡」「安全性・データの完全性(データインテグリティ)」「文書化」。 
SIEMENS SCADAでできること(製薬業界装置に求められる機能)

システム構築(システムインテグレーション)
IDECファクトリーソリューションズは、SCADAの専門的な構築能力と高度なシステムインテグレーション技術を保有しており、お客様のニーズに対応した最適なシステムを提供し、その効果的な運用の実現をサポートします。 システムインテグレータがSCADAシステムを構築する際には、以下のような技術力が求められます。IDECファクトリーソリューションズはそのすべてを提供することが可能です。
- SCADAソリューションの設計と構築に関する広範な経験と知識
- クライアントのニーズを理解し、それに基づいて最適なSCADAソリューションを実現する設計力
- SCADA技術の深い理解と適切な使用能力
- 大量のリアルタイムデータを効果的に収集、分析、処理する方法に関する深い知識
- 異なるシステムとデバイスを効果的に統合する能力
- システムの安全性とセキュリティを確保するための知識と技術
- プロジェクト管理スキルとクライアントとの良好なコミュニケーション能力
